摘要:煤层气转化制合成气工艺的生产成本低、能耗小,对减轻全球性温室效应具有一定的作用,是煤层气利用的较好方案,但该反应存在催化剂积炭严重易失活等问题。为此,采用Ni/MgO-Al203催化剂,在常压固定床反应器上进行了CO2重整CH4制合成气反应的研究,系统地考察了载体制备方法、MgO含量、焙烧方式等因素对催化剂性质的影响,并采用N2物理吸附和XRD检测手段对催化剂进行了表征。结果表明,采用共沉淀方法制备催化剂载体,当MgO含量为4%,在550℃流动空气环境里焙烧4h后所得到的催化剂10%Ni/4%MgO-Al203用于煤层气转化制合成气的反应,CH4和CO2的转化率分别可达到82%和92%,且反应6h内转化率没有降低,催化剂未发生积炭现象,其催化活性和稳定性都较好。
关键词:煤层气;CH4-CO2重整;催化剂;制备方法;MgO含量;焙烧方式;XRD
0 引言
煤层气主要成分与天然气基本相同[1],因此利用途径也很相似,大多用在民用燃气和发电上,有一小部分用作化工原料[2~5],但煤层气在开采过程中会混入一部分的空气,使其成分中除了CH4以外,还有一部分的CO2和O2,因此如何进一步高效利用这些气态碳氢资源已成为制约我国能源工业发展的重要环节。煤层气化工的起步比较晚,其研究工作是在天然气化工的基础上进行的。目前,利用煤层气制氢的生产工艺已经较为成熟,即利用甲烷与氧气的燃烧反应热,使甲烷与二氧化碳发生转化反应,得到含氢、CO、CO2和氮(煤层气中原有的)的混合气,然后通过变压吸附法一次除去所有杂质而得到纯氢[6~9];煤层气也可以作为燃料电池的燃料,尤其是磷酸盐燃料电池和高温固体燃料电池,可以减少能量的损失,但此工艺还需要克服很多技术难题[10];另外,开采中发现某些气田中CH4和C02的浓度很相近,可以直接作为CO2重整CH4反应的原料气制成合成气,再生产甲醇等一系列的化工产品[11~12],此工艺不仅生产成本低,能耗小,而且利用了廉价的煤层气,对减轻全球性温室效应也具有一定的作用。因此引起了各国科学家的兴趣。但该反应存在催化剂积炭严重易失活等问题,对此,科学家在天然气转化制合成气催化剂的研究基础上,进一步探索出一种适合煤层气重整反应的催化活性较高、抗积炭能力较强的催化剂是目前研究工作的重点[13~16]。
笔者采用Ni/MgO-Al203催化剂,对煤层气转化制合成气进行研究,系统考察了催化剂制备方法、MgO含量和焙烧方式等影响因素对载体催化剂性质的影响,并根据表征结果和其产物转化率的高低,确定出了一个活性较高的新型催化剂。
1 催化剂实验
1.1 催化剂的制备
分别采用沉淀-沉积法、共沉淀法和分步浸渍法制备4%MgO-Al203载体,以1:5(体积比)的氨水为沉淀剂,过程中pH值控制在10.5左右,连续搅拌2h,静置陈化5h,得到水凝胶,经过水洗和醇洗,抽滤之后得到醇凝胶,将所得的醇凝胶于110℃下干燥12h以上,焙烧制得载体;再改变MgO含量、焙烧方式等实验条件,制备出不同的载体。
采用浸渍法将适量的Ni(NO3)2·6H2O(纯度98.0%,开原化学试剂厂出产)浸渍到相应的载体上。催化剂于110℃干燥12h以上,焙烧,经压片,破碎,过筛至20~40目备用。
1.2 催化剂性能评价
催化剂性能评价在常压固定床反应装置MRCS-2000A上进行。催化剂的用量为200mg,放入石英反应管中(内径6mm)。先通入惰性气体(N2气)使催化剂床层温度升至设定温度。待温度稳定后通入体积比为1:9的H2/N2,在800℃下还原催化剂1h,然后再用氮气吹扫石英管15min,将管中的还原性气体吹扫干净。反应前先将气路阀拨至旁路以一定比例通入原料气,打开工作站检测气体比例是否正确。检查完毕后将气路旋转至反应档,通过皂沫流量计测量无水尾气的流量,催化剂床层温度即反应温度通过插入催化剂床层的热电偶测量,反应尾气经冷凝除水后,进入1790型气相色谱仪,以Ar为载气,用TCD检测器进行分析,柱温80℃,进样温度120℃,检测器温度110℃。待反应稳定后,每隔20min取样1次,用N-2000双通道色谱工作站进行检测数据处理和分析。
1.3 催化剂的表征
催化剂的比表面积及孔结构由ASAP-2020物理吸附仪(美国Micromeritics)测定。样品预先在350℃脱气5h,然后在-196℃进行N2吸附。比表面积用BET方程求得,孔体积取相对压力(p/p0,其中声为压力,Pa;p0为饱和点气压,Pa)为0.995时N2吸附量对应的体积、孔径分布根据脱附曲线利用BJH法求得。XRD谱图在BDX—2000型X射线衍射仪(北大青鸟)上进行,光源为Cu Kα靶,管电流20mA,管电压36kV,扫描范围衍射角2口为20°~75°。
2 实验结果与讨论
2.1 载体制备方法对催化剂性能的影响
分别采用沉积-沉淀法(DP)、浸渍法(Imp)和共沉淀法(CP)制备了4%MgO-Al203载体。制备方法对载体性质的影响结果见表1。
表1 不同方法制备4%MgO-Al203载体的物理性质比较表
|
制备方法
|
比表面积/m2·g-1
|
比孔容/cm3·g-1
|
平均孔径/nm
|
|
DP
|
174
|
0.7012
|
16.1
|
|
Imp
|
229
|
0.7387
|
12.9
|
|
CP
|
431
|
2.2020
|
20.4
|
从表1可以看出,不同方法制备载体的比表面积明显不同,共沉淀法制备载体的比表面积最大,可达到431m2/g,沉积-沉淀法和浸渍法制备载体的比表面积都较小。它们的比孔容差别也比较明显,由此可以看出,比表面积的大小与比孔容有关,比孔容越大,比表面积越大。
图1为沉积-沉淀法、浸渍法和共沉淀法制备4%MgO-Al203载体的吸附/脱附等温曲线。从图1中可以看出共沉淀方法制备的载体粒子N2吸附量最大,沉积-沉淀法和浸渍法的曲线基本相同。
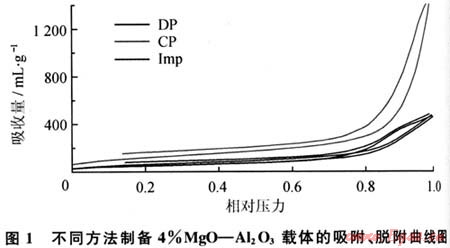
图2为不同方法制备4%MgO-Al203载体制成催化剂的XRD谱图。通过与标准谱图进行对比可以得知这3种催化剂中都存在Ni、Al、MgO、Al203、NiAl2O4相,其中,当2θ为36°处存在NiAl2O4尖晶石的衍射峰,共沉淀法制备的载体催化剂的NiAl2O4衍射峰最弱,而其他两种方法NiAl2O4的衍射峰逐渐增强,说明Ni与Al2O3的相互作用较强,使活性中心Ni的含量较少,进而影响其催化剂的催化活性。
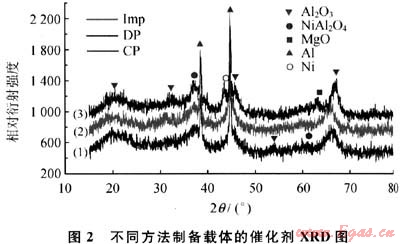
用不同方法制备4%MgO-Al203载体,用浸渍法负载Ni,制备成10%Ni/4%MgO-Al203催化剂,在常压固定床反应器中测得CHn的转化率(XCH4)和C02的转化率(XCO2)(图3、4)。从图3、4中可以看出,在反应开始阶段共沉淀法制备的载体催化剂的初始活性较高,可以超过90%,高于沉积沉淀法和浸渍法的催化活性,随着反应时间的进行,CH4和C02的转化率始终保持较高,但反应进行4h后,催化剂发生了积炭,催化活性有所降低,说明其稳定性不是很好。
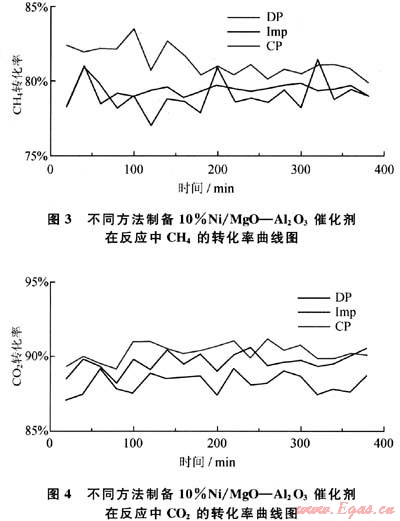
2.2 载体中MgO含量对催化性能的影响
采用共沉淀方法制备了4%MgO-Al203、7%MgO-Al203、10%MgO-Al203载体,不同MgO含量对载体性质的影响结果见表2。
表2 不同MgO含量MgO-Al203载体的物理性质表
|
载体
|
比表面积/m2·g-1
|
比孔容/cm3·g-1
|
平均孔径/nm
|
|
4%MgO-Al203
|
431
|
2.2020
|
20.4
|
|
7%MgO-Al203
|
591
|
2.4025
|
16.2
|
|
10%MgO-Al203
|
494
|
2.3108
|
18.7
|
从表2可以看出3种不同MgO含量的载体比表面积差别不是很明显,4%MgO-Al203载体的比表面积最小,7%MgO-Al203载体的比表面积较大,可以达到591m2/g,说明少量MgO的加入可以提高复合载体的比表面积,但随着加入量的增加,比表面积反而降低。
图5为共沉淀法制备MgO-Al203的孔径分布曲线。从图5中可以看出,3种不同MgO含量载体的孔径分布较为集中,主要在12nm,7%MgO-Al203、10%MgO-Al203的孔径和孔体积差不多,4%MgO-Al203载体的孔径和孔体积较小。
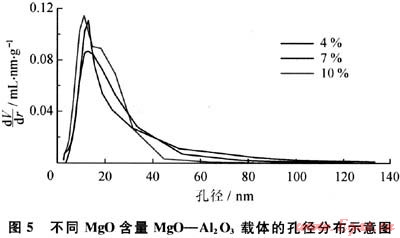
图6为不同MgO含量的载体催化剂的XRD谱图,通过与标准谱图对比可以看出,在2口为36°和62°两处出现NiAl2O4尖晶石的衍射峰,4%MgO-Al203载体曲线中NiAl2O4的衍射峰很弱,但随着MgO加入量的增加,NiAl2O4的衍射峰逐渐增强,说明Ni与Al2O3的相互作用增强,活性中心Ni逐渐减少,而且4%MgO-Al203载体的曲线比较散漫,表明粒径分布较为均匀,使得催化活性较好。
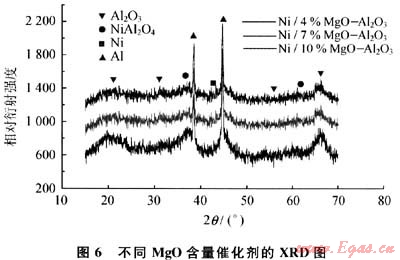
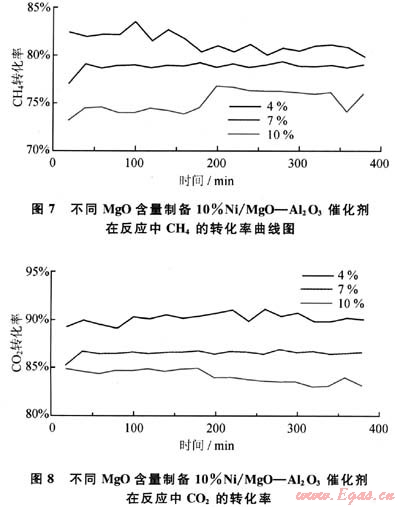
图7、图8为不同含量MgO-Al203载体制成10%Ni/MgO-Al203催化剂在反应中CH4和CO2的转化率。从图7、8中可以看出,在反应过程中10%Ni/4%MgO-Al203催化剂的催化活性最高,CH4和CO2转化率分别为82%和90%左右。随着反应的进行,10%Ni/4%MgO-Al203催化剂的催化活性略有浮动,但其转化率仍然较高,在整个反应过程中催化剂的催化活性变化都不是很大,表明其稳定性较好。
2.3 载体焙烧方式对催化剂性质的影响
分别采用静态空气(SAir)、流动空气(FAir)、流动氮气(FN2)焙烧制备4%MgO-Al203载体。不同焙烧方式对载体性质的影响结果见表3。从表3中可以看出,用流动空气焙烧的载体比表面积最大,可以达到537m2/g,静态空气焙烧的载体比表面积最小。
表3 不同焙烧方式制备4%MgO-Al203载体的物理性质表
|
焙烧方式
|
比表面积/m2·g-1
|
比孔容/cm3·g-1
|
平均孔径/nm
|
|
静态空气
|
431
|
2.2020
|
20.4
|
|
流动空气
|
537
|
1.9436
|
14.5
|
|
流动氮气
|
489
|
1.8757
|
15.4
|
图9为不同方式焙烧制备4%MgO-Al203载体的孔径分布曲线。从图中可以看出,3种不同焙烧方式所得载体的孔径分布主要集中在13nm,在流动空气和流动氮气焙烧方式下所得到的孔径和孔体积差不多,而在静态空气方式下焙烧的载体的孔径和孔体积较小,但其孔径的分布较为松散。
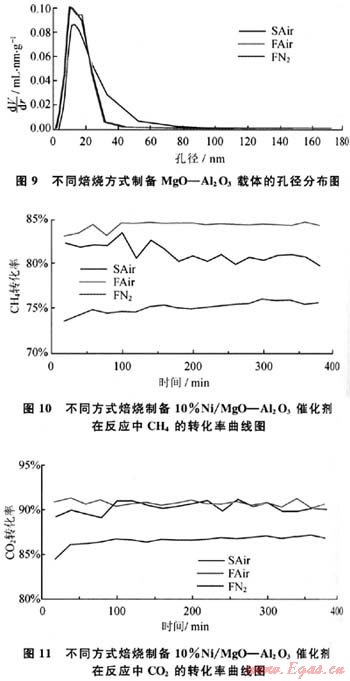
图10、图11为不同方式焙烧MgO-Al203载体制备10%Ni/ MgO-Al203催化剂在反应中CH4和CO2的转化率。从图10、11中可以看出,流动空气条件下焙烧载体催化剂的催化活性较好,CH4和CO2的转化率分别可以达到82%和92%左右,随着反应的进行,流动空气焙烧催化剂的催化活性一直较为稳定,表明催化剂的稳定性较好。
3 结论
通过对煤层气转化制合成气催化剂的研究发现:载体采用共沉淀方法制备,MgO含量为4%,在550℃流动空气环境里焙烧4 h所得到的催化剂10%Ni/4%MgO-Al203在煤层气转化制合成气的反应中,CH4和CO2的转化率分别达到82%和92%,反应的6h内二者的转化率没有降低,催化剂未发生积炭现象,表明催化剂的催化活性和稳定性较好,且该催化剂体系与天然气制合成气的催化剂体系相同。但煤层气CO2重整是一个强吸热反应,在反应过程中需要提供大量的热,若将放热的甲烷催化部分氧化和吸热的甲烷、二氧化碳重整结合起来制备合成气,不仅可以实现能量的耦合,降低反应能耗,还可以降低成本,而且煤层气中的氧气不需分离,可以直接作为CO2-O2联合重整CH4制合成气的反应原料,这方面工作有待于下一步进行研究。
参考文献
[1] 陈永武.中国天然气的发展和利用[J].当代石油石化,2004,12(11):24-26,44.
[2] 蒋孝兵,谢海英.煤层气利用新方案[J].天然气工业,2006,26(10):144-146.
[3] 孙万禄.我国煤层气资源勘探开发前景与对策[J].天然气工业,1999,19(5):1-5.
[4] 林金贵.我国煤层气研究开发的历史现状与趋势措施[J].科技资讯,2006(7):17.
[5] LOM W L.Liquefied natural gas[M].New York:HAL STED Press,1974:31-36.
[6] 陶鹏万,古共伟.利用煤层气制氢[J].天然气化工,2006,31(2):52-55.
[7] 唐晓东,孟英峰.变压吸附技术在煤层气开发中的应用探讨[J].中国煤层气,1996(1):46-49.
[8] 杨克剑.含氧煤层气的分离与液化[J].中国煤层气,2007,4(4):20-22.
[9] 张志翔,苑慧敏,王凤荣,等.煤层气的化工利用进展[J].现代化工,2007,27(8):26-29.
[10] 张强,顾瑶,徐益谦.以煤层气作为燃料的燃料电池发电技术[J].能源研究与利用,2000(6):32-35.
[11] 李琼玖,杜世权,廖宗富,等.实现零排放的煤层气利用最佳途径[J].中外能源,2006,11(6):15-20.
[12] 徐东彦,李文钊,葛庆杰,等.抽放煤层气(CH4-C02-Air)制合成气的研究——固溶体的形成对NiO/MgO催化剂性能的影响[J].燃料化学学报.2004,32(5):580-583.
[13] 欧阳朝斌,赵月红,郭占成.合成气制备工艺研究进展及其利用技术[J].现代化工,2004,24(6):10-13.
[14] 魏树权,周汉,李丽波,等.天然气二氧化碳空气和水蒸气制合成气的热力学研究[J].化学工程师,2003,95(2):21-23.
[15] 徐东彦,李文钊,陈燕馨,等.煤层甲烷部分氧化与CO2-H2O重整联合制合成气研究[J].煤炭学报,2004,29(3):468-471.
[16] 郑小明,莫流业,井强山,等.甲烷部分氧化与甲烷二氧化碳重整耦合制合成Co系催化剂研究[J].复旦学报:自然科学版,2003,42(3):253-256.
(本文作者:孙婷婷 周迎春 张启俭 李昊 齐平 辽宁工业大学化学与环境工程学院)
您可以选择一种方式赞助本站

支付宝转账赞助

微信转账赞助
